摘要:北卡羅來納大學醫學院生物化學和生物物理系的Susanna Stroik博士和Dale Ramsden博士對一種在遺傳性乳腺癌、卵巢癌和前列腺癌患者中過度表達的酶有了更多的了解。
我們的DNA不是堅不可摧的。在我們的一生中,DNA會因自然和環境因素而斷裂。值得慶幸的是,我們的身體有專門的酶和途徑,可以通過幾種不同的機制將破碎的DNA粘合在一起,這些機制被稱為DNA修復途徑。
然而,一些癌癥可以劫持這些途徑為自己的利益。Susanna Stroik博士和Dale Ramsden博士都是北卡羅來納大學醫學院和北卡羅來納大學Lineberger綜合癌癥中心生物化學和生物物理系的研究人員,他們拼湊出了一條鮮為人知的DNA修復途徑,稱為聚合酶θ介導的末端連接(TMEJ)。
在《自然》(Nature)雜志發表的一篇文章中,研究人員一步一步地闡述了這一途徑,這一途徑在許多遺傳性乳腺癌、卵巢癌和前列腺癌患者中,特別是在那些涉及 BRCA1 和 BRCA2 突變的患者中,被發現上調,而新的知識可能會帶來新的癌癥療法。
 圖1 聚合酶δ和θ在θ介導的末端連接的逐步需求
圖1 聚合酶δ和θ在θ介導的末端連接的逐步需求Ramsden實驗室的博士后研究員Stroik說:“患有這些乳腺癌突變的人,他們的癌癥依賴于聚合酶的修復途徑來保持腫瘤存活并修復癌組織中的DNA損傷。現在我們對這一途徑有了更多的了解,從理論上講,科學家們可以生產出一種藥物,可以破壞癌細胞中這一途徑的關鍵部分,而不是使用傳統的化療方法,在破壞癌癥的同時破壞健康細胞。”
聚合酶θ的發現
在所有DNA修復途徑中,TMEJ是最難以捉摸的。Richard Wood博士是德克薩斯大學MD安德森癌癥中心的杰出教授,他在2003年首次鑒定聚合酶theta中發揮了關鍵作用。
在接下來的15年里,包括Wood、Ramsden和Gupta實驗室(也在Lineberger綜合癌癥中心)在內的多個實驗室都能夠將聚合酶與DNA修復(TMEJ)和癌癥聯系起來。Sylvie doubli博士是北卡羅來納大學教堂山分校的校友,也是佛蒙特大學微生物學和分子遺傳學教授,她隨后解開了聚合酶θ的第一個結構。
這些研究人員與來自賓夕法尼亞州立大學和紐約大學的其他科學家一起,致力于準確地了解TMEJ中涉及的步驟,以及這些步驟中聚合酶θ起作用和不起作用的步驟。
在這些合作者的幫助下,Stroik能夠使用各種尖端的實驗方法來填補我們對TMEJ通路的理解空白。至至關重要的是,她發現另一種叫做聚合酶δ的聚合酶,與聚合酶θ一起使用一個伙伴系統來協助它完成這一修復途徑。
獨特的伙伴系統
Stroik的研究表明,聚合酶θ在某些方面表現出色,但在另一些方面卻不盡人意。
“它會產生很多錯誤,而且不能一次產生大量的DNA,”Stroik說。“整個發現的精妙之處在于,有兩種不同的酶在途徑步驟之間交替,相互幫助。”
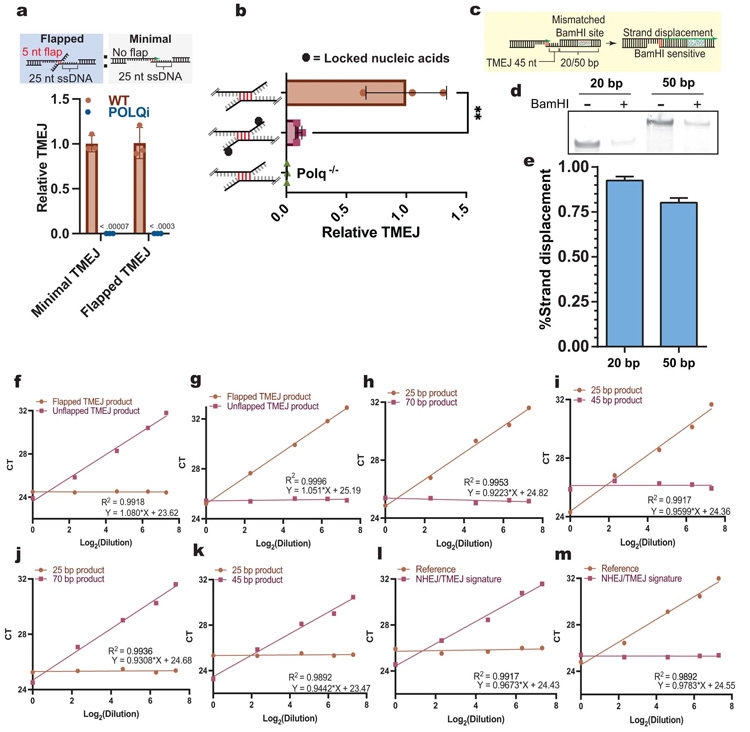 圖2 TMEJ的基本機制和驗證
圖2 TMEJ的基本機制和驗證當雙鏈斷裂發生時,兩條DNA鏈在同一點被剪斷,就像剪刀剪斷頭發一樣。聚合酶反應迅速,抓住兩條DNA單鏈,將最接近斷裂的堿基對配對,并將它們固定在一起。
然而,這通常會在末端留下一些單鏈DNA的殘余褶葉。聚合酶δ跳進去切斷多余的褶葉,給聚合酶θ足夠的空間開始合成新的DNA來填補DNA鏈上的空白。最后,聚合酶δ最后一次加入來幫助聚合酶θ完成合成。
Stroik還有另一個突破性的發現:聚合酶δ與聚合酶θ在物理上是相互連接的。這一新信息可能對希望通過藥物這種相互作用來創造一種新的癌癥治療方法的藥物開發人員特別有用。
癌癥治療潛力
由于許多癌癥利用TMEJ通路來維持腫瘤存活,許多研究人員已經在研究制造可以干擾該通路的藥物,從根本上阻止癌癥自我修復,導致其最終死亡。
Ramsden說:“任何時候你發現新的通路,你都可以‘給它下藥’。”
Stroik和Ramsden的新研究將為聚合酶θ和δ的基礎研究做出貢獻,同時也有助于目前處于臨床試驗中的稱為聚合酶θ抑制劑的新型抗癌藥物。
參考資料
[1] Stepwise requirements for polymerases δ and θ in theta-mediated end joining