腸道細菌自發躲避抗生素攻擊的“武器”
摘要:細菌用來轉移基因的超聚合物結構也可以在未來醫學中用于精確的藥物輸送。
腸道細菌形成稱為F-pili的細胞外附屬物,相互連接并傳遞稱為基因的DNA包,使它們能夠抵抗抗生素。人們認為,人類和動物腸道內的惡劣條件,包括湍流、熱量和酸,會破壞F-pili,使轉移更加困難。
然而,由倫敦帝國理工學院的研究人員領導的一個研究小組的新研究表明,在這些條件下,F-pili實際上更強壯,幫助細菌更有效地轉移抗性基因,并聚集成“生物膜”——保護性細菌聯合體——幫助它們抵御抗生素。這一發現說明了為什么對付耐藥細菌如此困難,但確實為解決這一問題提供了一條可能的途徑。細菌用來轉移基因的超聚合物結構也可以在未來醫學中用于精確的藥物輸送。研究結果發表在《Nature Communications》雜志上。

圖1 研究發現F-pili幫助細菌更有效地轉移抗性基因并聚集成“生物膜”
不同種類的細菌使用不同類型的pili在稱為結合的過程中轉移基因。一個經典的實驗似乎表明,這個過程是脆弱的,可能會被攪動打斷,但這留下了一個謎:如果腸道如此脆弱,為什么這么多生活在惡劣條件下的細菌會使用這些系統?
因此,研究小組開始驗證這一假設。通過搖動大腸桿菌,同時在接合過程中使用F-pili,他們發現攪拌實際上提高了細菌之間基因轉移的效率。他們還觀察到,在轉移基因后,在搖晃的條件下,結合的細菌更容易聚集在一起形成生物膜,從而保護內部細菌免受周圍抗生素分子的侵害。
為了確定F-pili是如何做到這一點的,研究小組對它們進行了強度測試,他們在一個臺上安裝了一個細菌,用“分子鑷子”將一個玻璃珠連接到其中一個F-pili的末端,然后拉。F-pili被證明是高度彈性的,具有彈簧般的特性,可以防止它們斷裂。
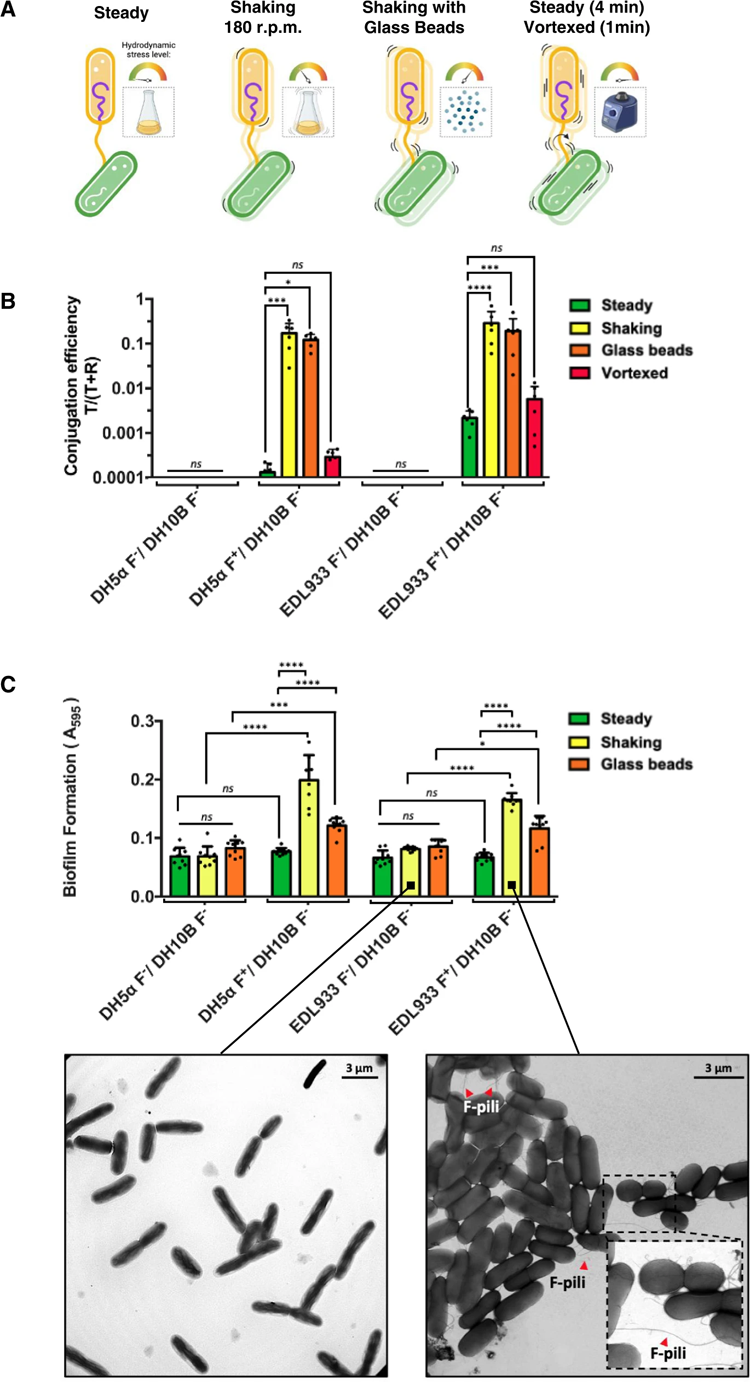
圖2 機械應力對結合效率和生物膜形成的影響。
他們還測試了F-pili對其他常見腸道條件的承受能力,將它們置于氫氧化鈉、尿素和100°C的高溫下——所有這些條件下F-pili都存活了下來。
然后,研究小組進一步研究了F-pili,從分子水平上觀察是什么賦予了它們這些令人難以置信的特性。它們主要由F-pilin“亞基”與相互連接的磷脂分子組成。
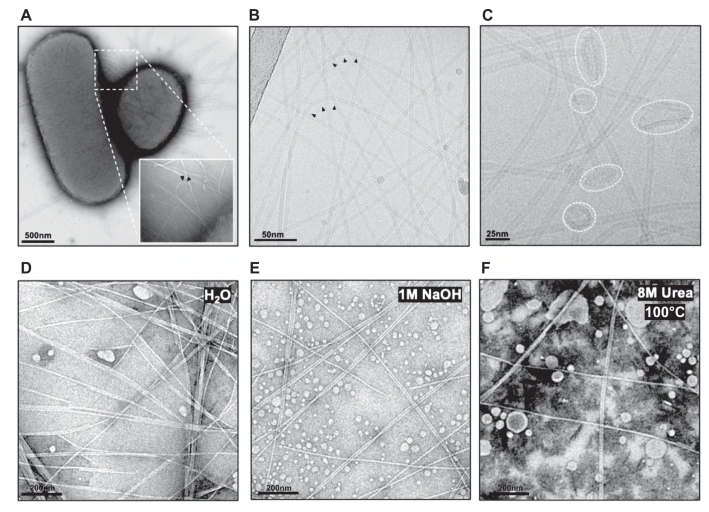
圖3 完整細菌和純化F-pili的電子顯微鏡顯微照片
通過模擬沒有磷脂的F-pili,研究小組展示了這些分子對結構的彈性和彈性強度有多重要。重復拉伸實驗表明,亞基在沒有磷脂支持的情況下迅速分解,證明了它們在長生物聚合物中作為“分子膠”的新作用。
來自帝國理工大學生命科學系的第一作者Jonasz Patkowski說:“到2050年,抗菌素耐藥性導致的死亡人數預計將與癌癥死亡人數持平,這意味著我們迫切需要新的策略來對抗這一趨勢。耐藥性的傳播在很大程度上是由細菌交換基因驅動的,因此對這一過程的詳細了解可能會導致中斷它的新方法。很難找到具有如此強大性能的管狀附屬物。細菌利用它來轉移基因,但如果我們能夠模仿這些特性,我們就可以使用類似的結構來精確地將藥物輸送到體內需要的地方”
來自帝國理工大學生命科學系的首席研究員Tiago Costa博士說:“就資源和能量而言,制造F-pili對細菌來說是非常昂貴的,所以它們值得付出努力也就不足為奇了。我們已經展示了F-pili如何在動蕩的環境中加速抗生素耐藥性的傳播和生物膜的形成,但現在的挑戰是找到對抗這一非常有效的過程的方法。”
雖然破壞致病菌中的F-pili是有利的,但如果我們能將它們用于藥物輸送等方面,它們的特性可能會有所幫助。
參考資料:
[1] The F-pilus biomechanical adaptability accelerates conjugative dissemination of antimicrobial resistance and biofilm formation
 |
 |
 |
| 官網:www.baichuan365.com | 微信服務號:iseebio | 微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn | 微信訂閱號:seebiotech | 泉養堂:www.canmedo.com |
下一篇:已經是最后一篇了上一篇: Nature子刊改變游戲規則:一種以前未知的細胞途徑
相關資訊
- 《科學》預測2015年重要突破
- JCB:科學家鑒別出轉移性前列腺癌的潛在治療靶點
- 西寶生物醫藥研究院裝修及配套項目設備采購公開競標
- 研究發現,冠狀病毒的形狀會影響其傳播
- Grace 923級硅膠 - GB/T11132及ASTM D1319專業推薦
- 研究發現,家族遺傳中重要的糖尿病基因!
- Cell子刊:腸道炎癥、感染的原因找到了,都是披薩漢堡惹的禍!
- Gastroenterology:關鍵的腸道干細胞基因或能將膳食脂肪與結腸癌風險聯系起來
- 蛋白類產品、鏈酶親和素和生物素衍生物
- 用于定量檢測PEG和PEG修飾性蛋白的ELISA試劑盒
新進產品
同類文章排行
- 腸道細菌自發躲避抗生素攻擊的“武器”
- Nature子刊改變游戲規則:一種以前未知的細胞途徑
- 黑發原來是這樣變白的!Nature最新研究發現逆轉白發的關鍵所在
- 新生蛋白質和隨機產生的蛋白質有什么不同?
- PNAS突破性新發現:幫助細菌在人類呼吸道定植的CPS特征
- 科學家們發現了可以減少抗生素對腸道細菌有害副作用的化合物
- “非凡的”促腦肽——MIT科學家發現逆轉阿爾茨海默病的方法
- Nature:血癌可以預防,關鍵在這個靶點
- Nature子刊:實時蛋白質分泌檢測技術
- mNGS在診斷血流感染方面優于常規微生物檢測
資訊文章
您的瀏覽歷史