摘要:肺癌腦轉移導致高死亡率,但轉移的確切機制尚不清楚。
2023年8月17日,廣州醫科大學何建行及克利夫蘭診所鮑仕登共同通訊在Cancer Cell 在線發表題為“CD44+ lung cancer stem cell-derived pericyte-like cells cause brain metastases through GPR124-enhanced trans-endothelial migration”的研究論文,該研究表明報道了肺腺癌(ADC)中來自CD44+肺癌干細胞(CSCs)的血管周細胞通過G蛋白偶聯受體124 (GPR124)增強的跨內皮遷移(TEM)引起腫瘤腦轉移。
在肺ADC中,血管周圍壁龕中的CD44+ CSCs生成了大部分血管周細胞。CSCs衍生的周細胞樣細胞(CD-周細胞)表現出顯著的TEM能力,可以有效地內滲到血管腔內,在循環中存活,外滲到腦實質,然后去分化為致瘤性CSCs形成轉移灶。CD-周細胞獨特表達GPR124,激活Wnt7-β-catenin信號,增強CD-周細胞的TEM內滲和外滲能力,這是腫瘤轉移的兩個關鍵步驟。此外,CD-周細胞、GPR124或Wnt7-β-catenin信號的選擇性破壞可顯著減少肺ADC的腦和肝轉移。該研究揭示了一種未被認識的驅動腫瘤轉移的細胞和分子模式。
 圖1 肺腺癌(ADC)中來自CD44+肺癌干細胞(CSCs)的血管周細胞通過G蛋白偶聯受體124 (GPR124)增強的跨內皮遷移(TEM)引起腫瘤腦轉移
圖1 肺腺癌(ADC)中來自CD44+肺癌干細胞(CSCs)的血管周細胞通過G蛋白偶聯受體124 (GPR124)增強的跨內皮遷移(TEM)引起腫瘤腦轉移腫瘤轉移是癌癥相關死亡的主要原因。超過90%的癌癥死亡可歸因于轉移。轉移是一個復雜的過程,有多個連續的步驟。內滲和外滲是癌細胞跨內皮遷移(trans-endothelial migration, TEM)跨越血管的關鍵過程。腫瘤轉移效率極低。只有那些有能力成功完成所有基本步驟的癌細胞才能最終導致可檢測的轉移。在轉移性癌癥中,肺癌在世界范圍內的死亡率很高。肺癌占所有腦轉移瘤的40-50%。
惡性肺癌在組織學上分為非小細胞肺癌(NSCLC,約占85%)和小細胞肺癌(SCLCs,約占15%)。非小細胞肺癌主要包括肺腺癌(ADC)、鱗狀細胞癌(SCC)和大細胞癌。大約50%的肺癌患者在疾病進展過程中發生腦轉移。盡管近年來在治療原發性肺癌方面取得了進展,但腦轉移患者的生存率仍然非常低。腦轉移治療的顯著失敗歸因于多種因素,包括腫瘤異質性、治療耐藥性和阻斷抗癌藥物有效遞送的血腦屏障(BBB),但對頻繁腦轉移機制的了解不足是一個明顯的障礙。
與大多數惡性腫瘤相似,肺ADC具有高度異質性,并含有癌癥干細胞(CSCs)。CSCs通常存在于血管周圍壁龕中,并與腫瘤微環境中的其他細胞和成分相互作用。盡管CD44、ALDH(醛脫氫酶)、CD133 (PROM1)和CD117 (KIT)等幾種上調標記物與肺ADC中的CSC特性相關,但CD44被廣泛用于識別肺ADC中的CSC。有報道稱,肺ADC中CD44表達與上皮-間質轉化(EMT)呈正相關。CSCs是促進惡性生長、治療抵抗和腫瘤復發的關鍵癌細胞。CSCs被提出可能通過EMT重編程促進腫瘤轉移,但CD44 CSCs究竟如何參與腫瘤轉移仍然難以捉摸。
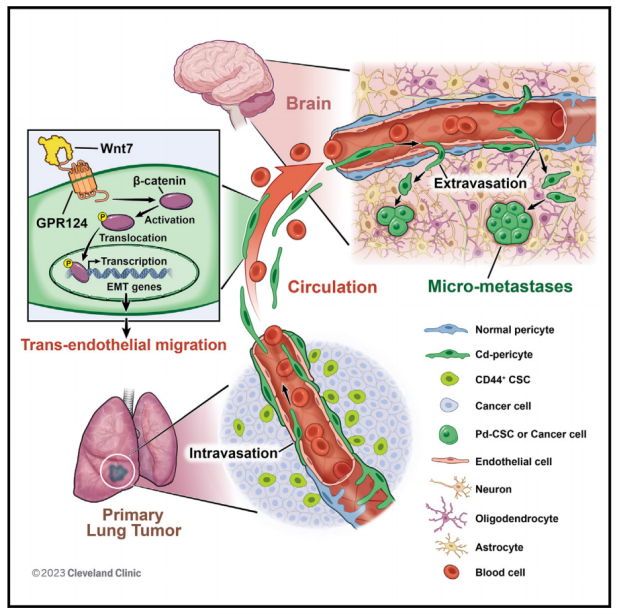 機理模式圖(圖源自Cancer Cell )
機理模式圖(圖源自Cancer Cell )該研究發現CD44+ CSC衍生的周細胞樣細胞(CD-周細胞)通過G蛋白偶聯受體124 (GPR124)介導的Wnt7-β-catenin信號傳導,顯示出強大的TEM內滲和外滲能力,從而導致腦轉移。總之,該研究揭示了一個未知的細胞模式和分子機制驅動腫瘤轉移,特別是肺ADC的腦轉移。由于乳腺癌等其他惡性腫瘤也會轉移到大腦,因此確定這里確定的機制是否適用于其他轉移性腫瘤將是非常有趣的。該研究為更好地了解腫瘤轉移打開了一扇獨特的窗口,也為預防或減少轉移提供了一種治療策略。
[1] CD44+ lung cancer stem cell-derived pericyte-like cells cause brain metastases through GPR124-enhanced trans-endothelial migration
 |
 |
 |
| 官網:www.baichuan365.com |
微信服務號:iseebio |
微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn |
微信訂閱號:seebiotech |
泉養堂:www.canmedo.com |