摘要:研究人員揭示了單胺類神經(jīng)遞質(zhì)如何通過這些單胺類神經(jīng)遞質(zhì)與組蛋白的化學(xué)結(jié)合。
西奈山和紀(jì)念斯隆凱特琳癌癥中心之間的合作努力,揭示了單胺類神經(jīng)遞質(zhì)(如血清素、多巴胺和組胺)如何通過這些單胺類神經(jīng)遞質(zhì)與組蛋白(我們細(xì)胞的核心DNA包裝蛋白)的化學(xué)結(jié)合,幫助調(diào)節(jié)大腦生理和行為。
通過揭示這些組蛋白修飾如何影響大腦,研究小組已經(jīng)確定了一種控制晝夜基因表達(dá)和行為節(jié)律的新機(jī)制。該團(tuán)隊(duì)的研究結(jié)果發(fā)表在1月8日星期三的《自然》雜志上,最終可能指導(dǎo)針對(duì)晝夜節(jié)律紊亂的疾病(如失眠、抑郁、雙相情感障礙和神經(jīng)退行性疾病)的靶向治療的發(fā)展。
 圖1 雙向組蛋白單胺化動(dòng)力學(xué)調(diào)節(jié)神經(jīng)節(jié)律
圖1 雙向組蛋白單胺化動(dòng)力學(xué)調(diào)節(jié)神經(jīng)節(jié)律“我們的研究結(jié)果強(qiáng)調(diào),大腦的內(nèi)部時(shí)鐘受到化學(xué)單胺類神經(jīng)遞質(zhì)以一種以前未被認(rèn)識(shí)到的方式的影響,例如單胺類可以直接修改組蛋白,而組蛋白反過來又調(diào)節(jié)大腦晝夜節(jié)律基因表達(dá)模式、神經(jīng)可塑性和睡眠或清醒活動(dòng)。”首席作者Ian Maze博士說,他是霍華德休斯醫(yī)學(xué)研究所研究員,西奈山伊坎醫(yī)學(xué)院神經(jīng)科學(xué)和藥理學(xué)教授,西奈山神經(jīng)表觀基因組工程中心主任。
“這一突破性的機(jī)制首次揭示了刺激大腦中神經(jīng)遞質(zhì)信號(hào)傳導(dǎo)(反之亦然)的晝夜節(jié)律事件如何通過直接改變DNA結(jié)構(gòu)對(duì)神經(jīng)元施加動(dòng)態(tài)影響,”Yael David博士補(bǔ)充道,他是一位化學(xué)生物學(xué)家,領(lǐng)導(dǎo)著紀(jì)念斯隆凱特琳癌癥中心的Yael David實(shí)驗(yàn)室,也是該研究的共同主要作者。“我們致力于更全面地了解這些機(jī)制,以便這項(xiàng)工作最終有助于開發(fā)治療晝夜節(jié)律相關(guān)疾病和其他腦部疾病的治療策略。”
迷宮實(shí)驗(yàn)室過去的研究發(fā)現(xiàn),血清素和多巴胺除了作為神經(jīng)遞質(zhì)(在神經(jīng)細(xì)胞之間傳遞信號(hào)的化學(xué)信使,控制著許多重要的身體功能)的作用外,還可以附著在組蛋白上,特別是H3。這些蛋白直接調(diào)節(jié)大腦中的基因表達(dá)程序,這些程序有助于復(fù)雜的生物過程和行為(包括神經(jīng)發(fā)育、藥物復(fù)發(fā)易感性和應(yīng)激易感性),并在受到干擾時(shí)導(dǎo)致疾病。實(shí)驗(yàn)室進(jìn)一步了解到,負(fù)責(zé)用血清素和多巴胺修飾組蛋白的酶是轉(zhuǎn)谷氨酰胺酶2 (TG2)。
在他們的最新研究中,來自納什家族神經(jīng)科學(xué)系、西奈山弗里德曼腦研究所和紀(jì)念斯隆凱特琳癌癥中心的研究人員使用了一種高度跨學(xué)科的方法來破譯TG2的生化機(jī)制。研究小組發(fā)現(xiàn),TG2作為細(xì)胞內(nèi)單胺類神經(jīng)遞質(zhì)的調(diào)節(jié)劑,不僅能將單胺類神經(jīng)遞質(zhì)添加到組蛋白H3上,還能在H3上擦除和交換一種單胺類神經(jīng)遞質(zhì),不同的單胺通過獨(dú)立的機(jī)制控制基因表達(dá)模式。
“這個(gè)想法源于對(duì)TG2及其輔助因子形成的化學(xué)中間體的簡(jiǎn)單觀察,揭示了一種新的動(dòng)態(tài),”該研究的第一作者Qingfei Zheng博士說,他曾是David實(shí)驗(yàn)室的博士后,現(xiàn)在是普渡大學(xué)的一名教員。
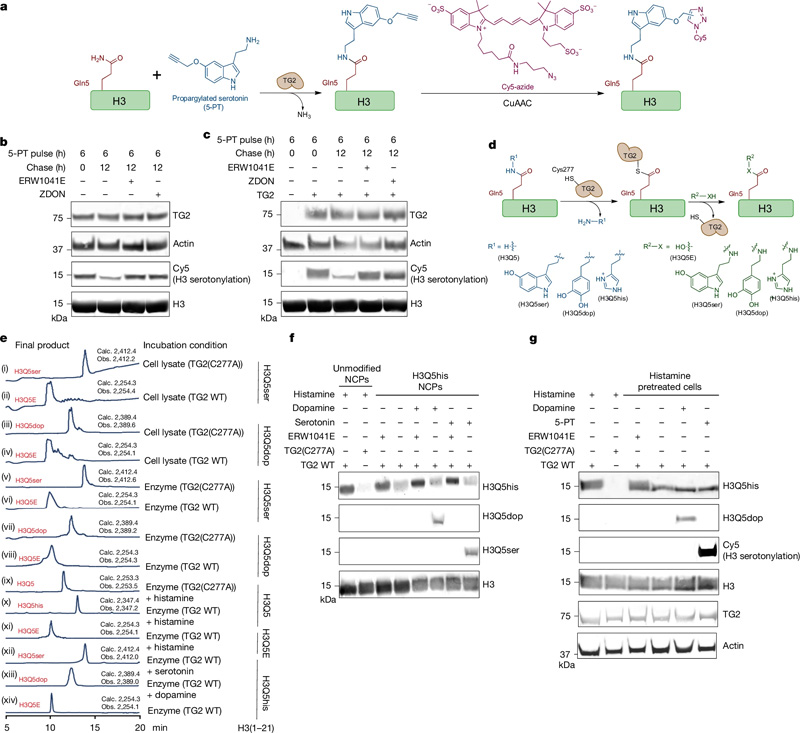 圖2 TG2是H3單胺基化的寫入、擦除和交換工具
圖2 TG2是H3單胺基化的寫入、擦除和交換工具Maze博士解釋說:“這些發(fā)現(xiàn)是同類研究中的第一個(gè),這意味著大腦的多個(gè)區(qū)域可以容納異質(zhì)性的單胺,它們可能會(huì)在外部刺激下迅速交換組蛋白上的單胺,從而直接調(diào)節(jié)基因表達(dá)程序。”
“這種獨(dú)特的機(jī)制表明,額外的組蛋白單胺修飾可能是動(dòng)態(tài)調(diào)節(jié)的,可能在控制大腦中的復(fù)雜事件中發(fā)揮作用,”David博士補(bǔ)充說。
基于這種新的作用機(jī)制,研究小組推測(cè)細(xì)胞內(nèi)單胺濃度的波動(dòng)可能導(dǎo)致它們被TG2選擇性利用,從而引發(fā)新的組蛋白修飾。事實(shí)上,研究人員發(fā)現(xiàn)組胺化(指TG2與代謝性供體組胺的反應(yīng))是組蛋白的一種新的修飾,并表明它與相關(guān)的H3 - 5 -羥色胺化過程一起,在調(diào)節(jié)小鼠大腦的晝夜節(jié)律和晝夜行為中起著關(guān)鍵作用。
“組胺化還表明,我們的大腦如何控制睡眠/覺醒周期是一種新的神經(jīng)傳遞獨(dú)立機(jī)制,而睡眠/覺醒周期在許多疾病中都被打亂了,”Maze博士說。
考慮到組胺在其他生物過程和疾病狀態(tài)中發(fā)揮的關(guān)鍵作用,包括免疫系統(tǒng)調(diào)節(jié)和癌癥,研究人員現(xiàn)在對(duì)進(jìn)一步探索如何控制TG2依賴性組蛋白單胺化感興趣。
“通過闡明TG2調(diào)節(jié)機(jī)制,我們可能能夠?qū)伟纺苁д{(diào)疾病,包括抑郁癥、精神分裂癥和帕金森病,獲得有價(jià)值的見解。我們的工作真正代表了一項(xiàng)基礎(chǔ)研究,有望導(dǎo)致更先進(jìn)的人類研究,具有重要的治療意義,”Maze博士總結(jié)道。
參考資料
[1] Bidirectional histone monoaminylation dynamics regulate neural rhythmicity
 圖1 雙向組蛋白單胺化動(dòng)力學(xué)調(diào)節(jié)神經(jīng)節(jié)律
圖1 雙向組蛋白單胺化動(dòng)力學(xué)調(diào)節(jié)神經(jīng)節(jié)律