《Nature Protocols》:新突破!能夠模擬人類胚胎植入的模型
摘要:奧地利科學院分子生物技術研究所創建用于模擬早期人類胚胎的人胚狀體
人類的早期發展為胚胎和成年生命奠定了基礎,但此領域仍然難以研究。一個解決方案來自于干細胞組織成類似于植入前胚胎的結構的能力——稱之為胚細胞。2021年奧地利科學院分子生物技術研究所的Nicolas Rivron研究團隊發表在Nature的一篇文章報道了一個用于模擬早期人類胚胎的人胚狀體,該研究團隊利用人多能干細胞構建了人胚泡樣結構(胚狀體)。作者鑒定出Hippo、TGF-β和ERK三個信號通路,抑制它們就能得到有效模擬正常胚泡發育(成功率>70%)和能形成正確細胞(成功率>97%)的胚狀體。

圖 2021年研究團隊利用人多能干細胞構建了人胚泡樣結構
在此基礎上,該團隊進一步描述了如何形成人類母細胞,這些母細胞可以(1)有效地實現囊胚的形態和(2)根據囊胚發育的速度和順序形成譜系,(3) 最終形成轉錄反映囊胚的細胞(植入前階段)。總之,母細胞提供了一個機會,可以為早孕建立科學和生物醫學發現計劃,并提供一種替代胚胎使用的倫理選擇。
相關研究成果以“Generating human blastoids modeling blastocyst-stage embryos and implantation”為題于2023年2月15日發表在Nature Protocols上。

圖 2023年研究團隊描述了如何形成人類母細胞
01 抑制Hippo、ERK和TGFβ通路
在4 dpf時,孕體形成桑葚胚,啟動空化形成囊胚。囊胚發育(5-7 dpf)支持三個創始譜系的產生:外胚層(EPI),它是胚胎的;滋養外胚層(TE),是胚外的;和原始內胚層 (PrE),它是胚外的(圖1a)。外周細胞通過抑制 Hippo 通路變成TE。在PXGL2中培養的原始人多能干細胞(PSC)在抑制TGFβ和ERK通路后有效地形成TE類似物。該團隊在非粘附水凝膠微孔中聚集初始PSC并抑制這三種途徑(圖1b)。在含有STAT激活劑白血病抑制因子(LIF)和Y-27632(一種 ROCK 抑制劑),囊胚樣結構有效形成(圖1c-e)。
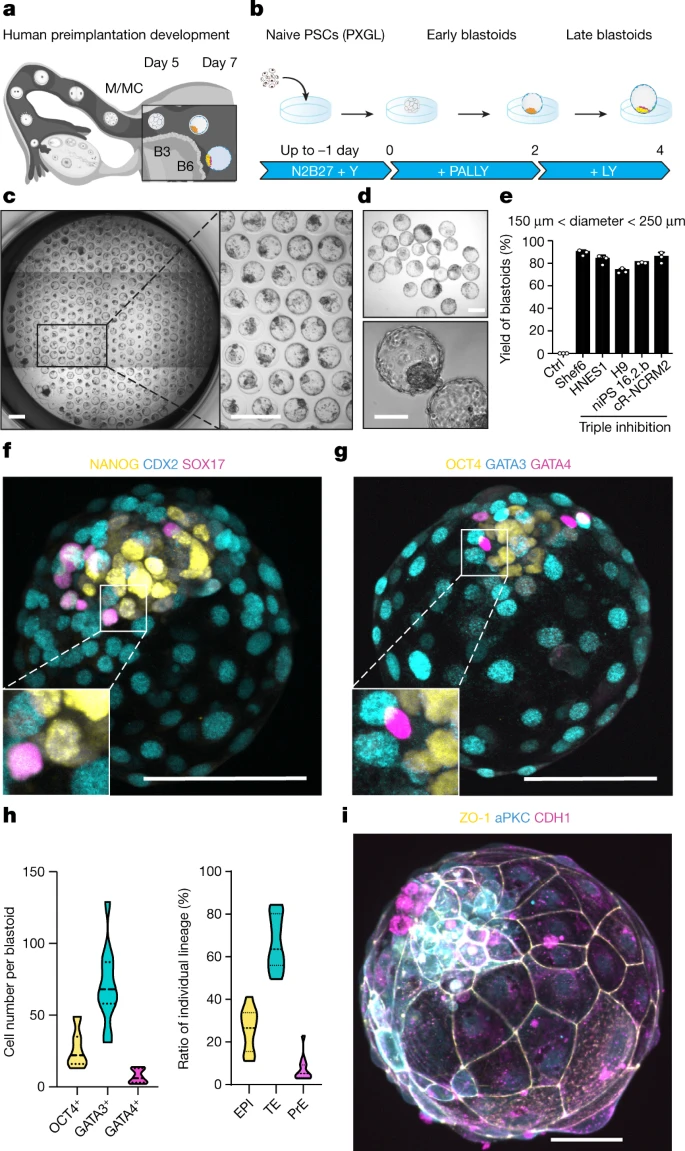
圖1 三重抑制的幼稚 PSC 有效地形成了人類胚泡樣結構,其中包含三個創始譜系的類似物
02 囊胚期類似物的形成
單細胞轉錄組學分析表明,胚泡樣結構僅形成三種不同的轉錄組狀態(圖2a、b),由三個創始譜系特有的基因標記,包括GATA2和GATA3 (TE)、POU5F1和KLF17 (EPI),以及GATA4 和SOX17 (PrE)(圖2c、d)。與來自胚泡、體外培養的胚泡和原腸胚形成期胚胎的細胞比較表明,胚泡樣結構中的細胞在轉錄上與胚泡期相似并且不同于著床后階段(圖2e、f)。
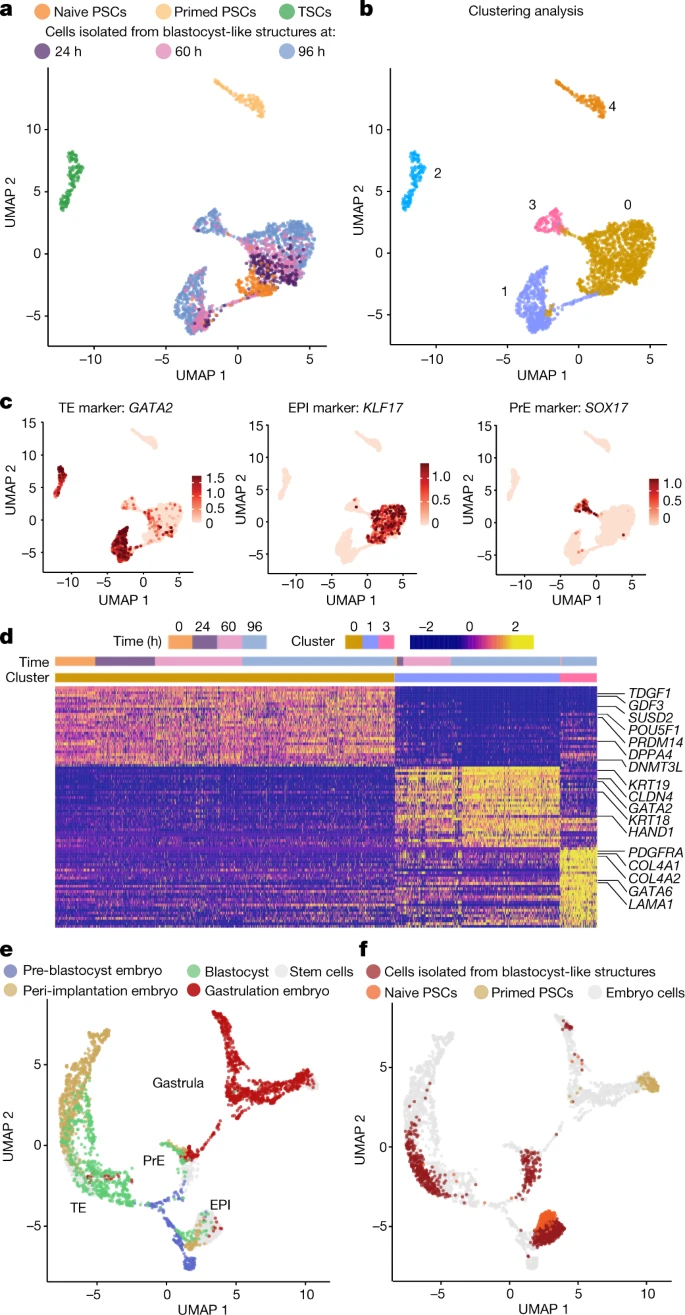
圖2 人類胚泡樣結構形成三種植入前譜系的類似物
03 Hippo抑制必不可少
關于人類囊胚譜系分離的知識是有限的(圖3a)。然而,已知在獲得頂端結構域后外周細胞中會發生Hippo通路的抑制,并且需要啟動TE規范。因而作者測試了囊胚樣結構是否采用了這種機制。值得注意的是,aPKC和F-肌動蛋白表達域在外部細胞中似乎是共同排列的,這些細胞也在細胞核中積累了Hippo下游效應子YAP1。YAP1核位置與GATA2和GATA3表達相關,與NANOG表達形成對比,并且僅限于TE類似物(圖3b)。aPKC抑制劑可以抑制Hippo通路的LPA受體配體(LPA和NAEPA)增強了囊胚樣結構的形成(圖3c)。由于Hippo通路抑制釋放YAP1進入細胞核,作者測試了YAP1的基因工程水平和功能是否會影響形態發生。YAP1 (5SA)的野生型或組成型活性形式的過表達加速了空化(圖3d)。
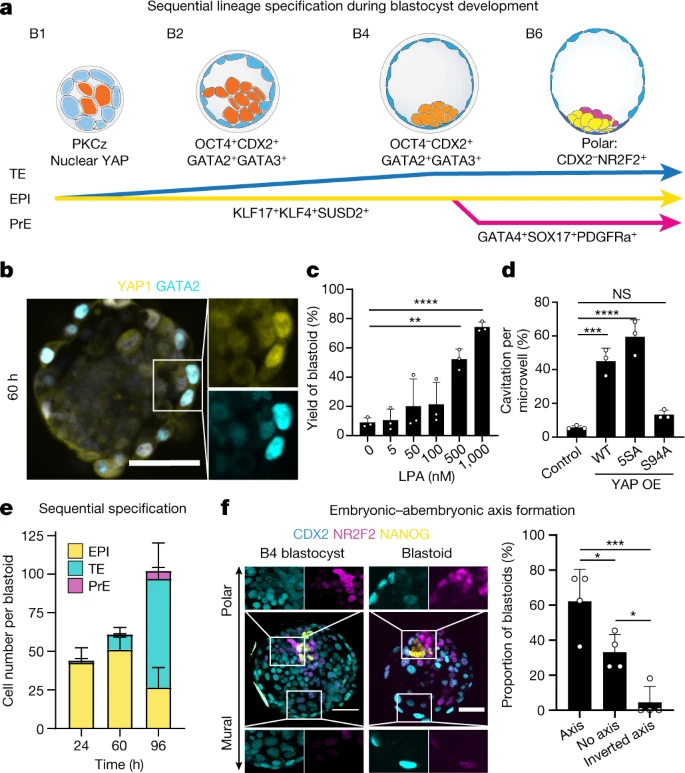
圖3 根據囊胚發育的順序和時間形成三個譜系
04 明顯附著于子宮內膜細胞
在7 dpf時,人類囊胚通過其TE附著到接受性子宮內膜開始在子宮內著床(圖4a)。作者測試了母細胞是否可以通過在2D中接種子宮內膜類器官來模擬這種相互作用,以形成一個開放的子宮內膜層(OFEL)以促進母細胞的沉積(圖 4a)。沉積在未受刺激的OFEL上的母細胞沒有附著;然而,它們確實附著并排斥受刺激的OFEL的子宮內膜細胞,就像在子宮內發生的那樣(圖4b)。由此得出結論人類母細胞能夠與已經接受的子宮內膜細胞特異性相互作用。
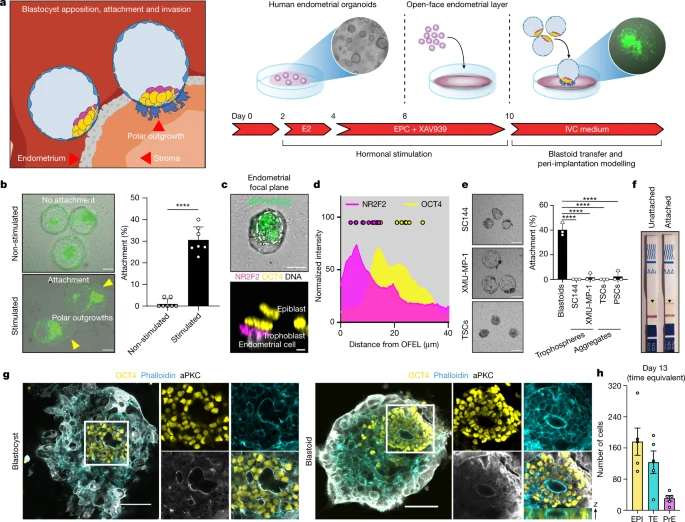
圖4 人類母細胞概括了植入的各個方面
綜上,人類母細胞在形態上類似于人類囊胚,有效地生成其三個譜系的類似物,其轉錄組與人類囊胚階段相匹配,并根據序列(TE和EPI,然后是pTE和PrE)和近似速度形成這些類似物(4天)胚泡發育。
因此,作者建議該模型與人類囊胚發育和植入的研究相關。模擬外胚層和滋養外胚層之間的相互作用表明,外胚層誘導極地滋養外胚層的局部成熟并隨后賦予它附著在受刺激的子宮內膜細胞上的能力。將來,人類胚細胞可用于幫助確定治療靶點并有助于臨床前建模(例如,體外受精培養基補充劑,如LPA和NAEPA或避孕藥,如SC144)。考慮到人類胚胎學的相稱性(平衡利弊)和輔助性(使用道德上問題最少的手段追求目標),胚細胞代表了一個倫理機會來補充使用胚胎的研究。
參考資料:
[1]Heidar Heidari Khoei, Alok Javali, Harunobu Kagawa, Theresa Maria Sommer, Giovanni Sestini, Laurent David, Jana Slovakova, Maria Novatchkova, Yvonne Scholte op Reimer & Nicolas Rivron, Generating human blastoids modeling blastocyst-stage embryos and implantation,Nature Protocols (2023)
[2]Harunobu Kagawa, Alok Javali, Heidar Heidari Khoei, Theresa Maria Sommer, Giovanni Sestini, Maria Novatchkova, Yvonne Scholte op Reimer, Gaël Castel, Alexandre Bruneau, Nina Maenhoudt, Jenna Lammers, Sophie Loubersac, Thomas Freour, Hugo Vankelecom, Laurent David & Nicolas Rivron, Human blastoids model blastocyst development and implantation, Nature volume 601, pages600–605 (2022)
[2]Harunobu Kagawa, Alok Javali, Heidar Heidari Khoei, Theresa Maria Sommer, Giovanni Sestini, Maria Novatchkova, Yvonne Scholte op Reimer, Gaël Castel, Alexandre Bruneau, Nina Maenhoudt, Jenna Lammers, Sophie Loubersac, Thomas Freour, Hugo Vankelecom, Laurent David & Nicolas Rivron, Human blastoids model blastocyst development and implantation, Nature volume 601, pages600–605 (2022)
 |
 |
 |
| 官網:www.baichuan365.com | 微信服務號:iseebio | 微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn | 微信訂閱號:seebiotech | 泉養堂:www.canmedo.com |
下一篇:已經是最后一篇了上一篇: 解碼微生物腸道信號的研究為IBD提供了潛在的新治療方法
相關資訊
- Small:重磅!科學家成功利用免疫細胞運輸抗癌藥物至腫瘤靶點
- 2020年4月3日,全球COVID-19確診病例累計突破100萬!
- J Med Chem:HIV藥物依法韋侖或有望治療阿爾茲海默病
- Analytica 2012 Part 9 - 低聚糖 Oligosaccharides
- CHO宿主細胞蛋白生物素標記多抗
- 氫氧化鋅|20427-58-1|Zinc hydroxide-己內酰胺工藝專用
- Cell:為何免疫系統檢測不到癌癥?
- 食品藥品監管總局發布生物類似藥研發與評價技術指導原則
- Nature點評:兒童和成人一樣易感新型冠狀病毒
- 西寶生物2016年2月生日會
新進產品
同類文章排行
- 《Nature Protocols》:新突破!能夠模擬人類胚胎植入的模型
- 解碼微生物腸道信號的研究為IBD提供了潛在的新治療方法
- 《Nature Immunology》兩種不同類型的免疫細胞幫助20億人控制結核病
- Molecular Cell令人驚訝的發現:導致抗生素耐藥性的第一步
- 研究發現,這種“升級版”輔酶Q10能逆轉HIV引起的器官損傷
- 《Cell》發育中的神經細胞利用必需氨基酸的機制
- 淋巴細胞性脈絡叢腦膜炎病毒(LCMV)研究新進展
- Nature Methods:新的亮紅色熒光蛋白
- Nature子刊發現全新機制:新的凝血調節機制
- Nature子刊:血管周圍細胞誘發阿爾茨海默病相關的微膠質功能障礙
資訊文章
您的瀏覽歷史