Nature:要想形成長期記憶,必須有DNA損傷和腦部炎癥?!

圖1 通過DNA感應TLR9途徑形成記憶組件
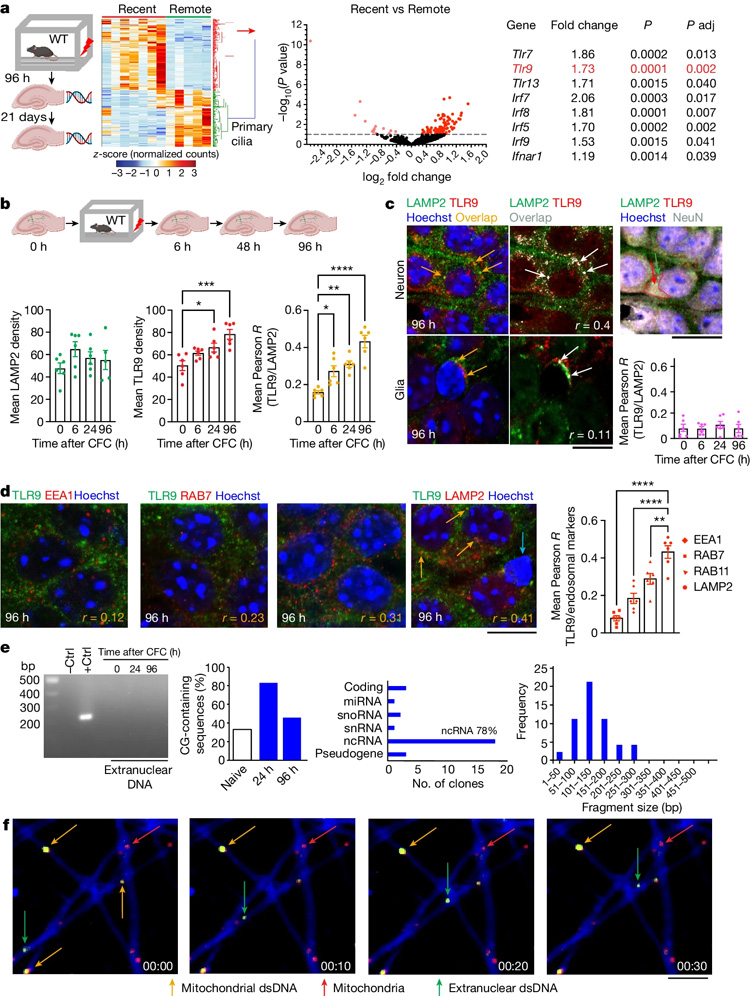
圖2 CFC后的核酸傳感活性
 |
 |
 |
| 官網:www.baichuan365.com | 微信服務號:iseebio | 微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn | 微信訂閱號:seebiotech | 泉養堂:www.canmedo.com |
相關資訊
- 人iPS細胞來源的多巴胺神經細胞,人神經細胞疾病模型 ReproNeuro DA
- 首例老年癡呆癥,帕金森癥活體檢測技術
- Jackson ImmunoResearch AffiniPure 大鼠抗小鼠 IgG (H+L) (min X Hu, Bov, Hrs, Rb, Rat Sr Prot)產品線停售通知
- 透明質酸衍生物 Hyaluronic acid derivatives
- 西寶生物邀您8月共赴深圳國際檢驗醫學及體外診斷試劑展覽會
- 超52萬人研究數據揭示:每天都在攝入的食用油,怎么吃才更健康?
- mRNA疫苗技術解析-關鍵性原料為開發保駕護航
- 輔助生殖上熱搜了!第三代試管嬰兒技術迎來“世紀機遇”
- 鴨子出現變異禽流感病毒亞型
- 神經退行性疾病新型療法出爐!《iScience》提示脂肪細胞或可有效改善認知功能下降
新進產品
同類文章排行
- Nature:要想形成長期記憶,必須有DNA損傷和腦部炎癥?!
- 《Nature》新型抗體治療讓衰老的免疫系統恢復了年輕
- 發現阿爾茨海默病的新治療靶點PDE4B 活性降低27%可大大挽救AD小鼠記憶、大腦功能和炎癥
- Cell子刊開辟衰老研究新方向:“垃圾蛋白”的積累被認為是衰老的關鍵原因
- 白色念珠菌毒素在消化道定植中起著特殊的作用
- Nature:在果蠅中,一個腦細胞可以驅動身體的多種運動
- Nature Metabolism:胰島素影響細胞能量的循環利用
- Cell子刊:抗凋亡MCL-1在線粒體代謝中的作用
- Science Immunology發現負責快速免疫反應的關鍵代謝過程
- 糖尿病治療的里程碑——轉基因奶牛產“人胰島素”奶
資訊文章
您的瀏覽歷史