Nature子刊:血管周圍細胞誘發阿爾茨海默病相關的微膠質功能障礙
摘要:小膠質細胞是保護哺乳動物大腦的初級免疫細胞,部分是通過吞噬病原體和有毒碎片來實現的。最近的遺傳學研究一直強調小膠質細胞在發育中的作用。
小膠質細胞是保護哺乳動物大腦的初級免疫細胞,部分是通過吞噬病原體和有毒碎片來實現的。最近的遺傳學研究一直強調小膠質細胞在阿爾茨海默病(AD)和其他神經退行性疾病發展中的作用,表明它們可以異常地開始吞噬突觸,神經元之間的關鍵連接。現在,倫敦大學學院(UCL)英國癡呆癥研究所的研究人員進行了一項研究,旨在更好地了解小膠質細胞可以增加患AD風險的吞噬過程。
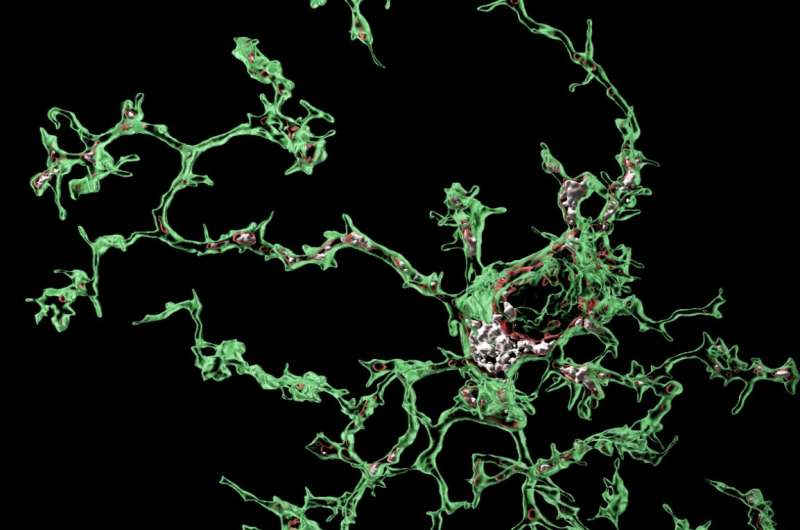
“在大腦發育的過程中,小膠質細胞吞噬突觸需要被移除,才能使大腦正常連接,”該研究的小組負責人、通訊作者Soyon Hong博士說。“然而,當大腦遭受疾病或衰老時,小膠質細胞的這一關鍵功能可能會重新激活,導致異常的吞噬和突觸的丟失。我們是第一批在模擬AD某些方面的小鼠模型中顯示小膠質細胞以特定區域的方式過量攝取突觸的團隊之一。這是相關的,因為突觸喪失是人類AD患者認知障礙的最強相關因素之一。”
雖然在AD小鼠模型中,阻斷突觸的小膠質細胞吞噬可以防止突觸的丟失,但觸發這種不良吞噬過程的信號仍然是一個謎。在這項發表在《Nature Neuroscience》雜志上的新研究中,由博士后科學家Sebastiaan De Schepper博士領導的團隊揭示了小膠質細胞和鄰近的血管周圍巨噬細胞(一種排列在小血管上的細胞)之間前所未有的通信,發生在突觸吞噬之前。

圖1 研究人員揭示了小膠質細胞和鄰近的血管周圍巨噬細胞之間前所未有的通信
“我們發現了血管周圍巨噬細胞在突觸病理中的驚人作用,”De Schepper博士解釋道。“在正常的大腦中,血管周圍的巨噬細胞在血液中巡邏,尋找潛在的病原體,但現在看來,它們也對血管周圍淀粉樣蛋白的早期積累做出反應。”
β淀粉樣蛋白是一種存在于大腦神經元細胞中的蛋白質。當這種蛋白質積累太多時,它會形成稱為“斑塊”的團塊,這是AD的病理標志。
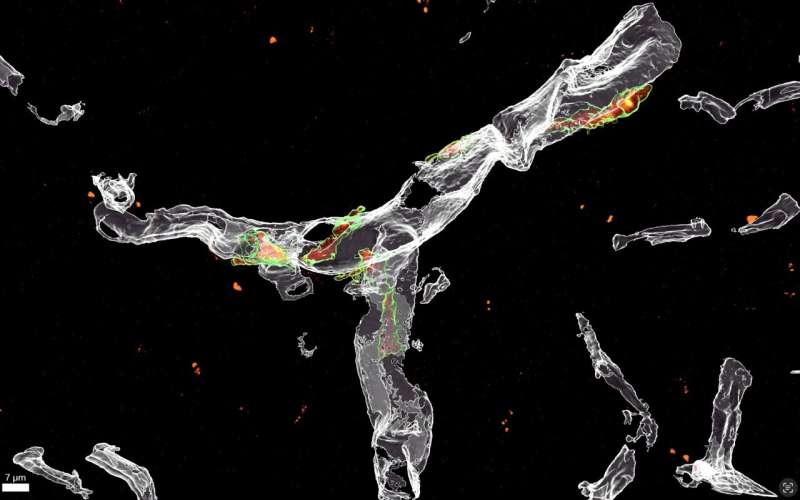
“然而,越來越清楚的是,β淀粉樣蛋白在疾病早期聚集在血管周圍,促使局部細胞,如血管周圍巨噬細胞,啟動免疫反應,”De Schepper博士補充道。
在AD小鼠模型中使用最先進的顯微鏡技術,De Schepper博士和Hong博士特別發現,這種免疫反應需要釋放SPP1,或骨橋蛋白,一種作為免疫調節劑的糖蛋白,導致小膠質細胞吞噬突觸的激活。De Schepper博士進一步解釋說:“值得注意的是,SPP1此前已被發現在AD患者的腦脊液中高表達,但直到現在還不知道它的功能。血管周圍巨噬細胞釋放SPP1可能代表了預測大腦免疫系統如何對AD早期病理改變做出反應的新治療途徑。”倫敦大學學院的Hong實驗室進行的這項研究的一個超額目標是精確定位導致早期AD患者突觸喪失的小膠質細胞亞型。他們的新研究朝著這個方向又邁進了一步,因為它幫助他們闡明了一些與小膠質細胞功能脫軌有關的過程。
Hong博士解釋說:“不同小膠質細胞和血管周圍亞群的鑒定和表征將對AD中突觸的保存具有重要的治療意義。我們假設,一種潛在的亞型可能以促炎糖蛋白SPP1(骨橋蛋白)的高表達為特征。在體內,SPP1在多個器官中標記許多吞噬性巨噬細胞亞型。在大腦中,SPP1還標記參與吞噬的小膠質細胞和血管周圍巨噬細胞,包括突觸。”
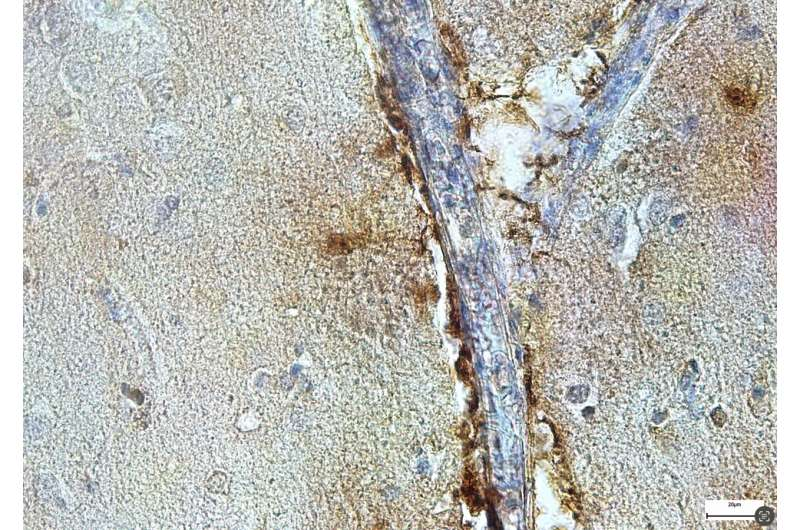
隨后使用單細胞RNA測序技術,這種方法使我們能夠研究大腦單個細胞中活躍的基因。他們發現血管周圍細胞通過SPP1主動指示小膠質細胞吞噬突觸。在下一步中,他們使用遺傳技術從小鼠中去除SPP1基因。這使他們能夠確定SPP1的缺失是否可以阻止小膠質細胞吞噬重要突觸的不受歡迎的過程。
事實上,來自缺乏SPP1的小鼠的小膠質細胞(“SPP1 -敲除小鼠”)被阻止吞噬突觸,這表明這種蛋白質是發生小膠質細胞吞噬所必需的。這組研究人員最近收集的結果證實了以前的發現,暗示血管空間在AD中的中心作用。
Hong博士解釋說:“我們的研究結果支持了早期的研究,這些研究強調了大腦中的血管細胞是淀粉樣β蛋白沉積物早期形成的關鍵部位。這反過來可能引發SPP1的增加,這可能導致血管周圍細胞向鄰近的小膠質細胞發出信號,誘導與AD相關的突觸過度進食。”
有趣的是,在他們的研究中,De Schepper博士和團隊還在已故AD患者的海馬血管周圍細胞中檢測到了SPP1,這意味著他們在小鼠身上的結果也適用于人類。因此,他們的發現可能很快就會為AD的新治療干預的發展提供信息,這些治療干預旨在通過血管周圍空間調節小膠質細胞的活動。
“我們現在正在測試不同的方法來治療AD早期階段的SPP1,旨在防止大腦中的突觸喪失和炎癥,”De Schepper博士補充道。“一種方法是通過所謂的‘反義寡核苷酸’(ASO)。ASO是遺傳物質的小片段,被設計成與體內特定的RNA分子結合。我們與Ionis制藥公司一起開發了一種ASO,它專門與SPP1結合并干擾其產生,我們希望這將有助于將我們的發現轉化為AD突觸保存的新治療方法。”
參考資料:
[1] Perivascular cells induce microglial phagocytic states and synaptic engulfment via SPP1 in mouse models of Alzheimer’s disease
 |
 |
 |
| 官網:www.baichuan365.com | 微信服務號:iseebio | 微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn | 微信訂閱號:seebiotech | 泉養堂:www.canmedo.com |
相關資訊
- 基因技術有助HIV疫苗開發
- Cell Rep:細胞衰老與年齡相關的血塊有關
- 華人自述:感染新冠BA.5后咳血難忍,BA.5抗性是mRNA疫苗的4倍!迄今最糟糕的變異版本
- 食物中毒致病菌收集用磁石NH顆粒系列 O157、O26、O111
- 西寶生物邀您共赴第20屆世界制藥原料中國展(CPhI china 2020)盛會
- 西寶生物參展2016年慕尼黑上海分析生化展回顧
- 中國學者發現胃癌診斷潛在標志物 或有助于胃癌診斷治療
- Science Advances新突破:快速高效生產人體免疫細胞的新方法
- Nat Com:最新研究找到調節心臟及肌肉關鍵蛋白的機理
- 乳糖/D-半乳糖[快速]檢測試劑盒
新進產品
同類文章排行
- Nature子刊:血管周圍細胞誘發阿爾茨海默病相關的微膠質功能障礙
- 是什么殺死了貝多芬?Cell子刊最新研究利用貝多芬的基因組找到了線索
- 確定了導致SARS-CoV-2感染的人類基因——CIART
- CAR-T療法創始人PNAS發文:實體腫瘤治療曙光出現?利用“組合拳”幫助T細胞
- 神經信號調節新發現:L-或D-氨基酸?鏡像分子可改變神經元的信號!
- 一個全新的抗生素世界!Nature子刊報道單個噬菌體蛋白特性研究新方法
- 《科學》:諾獎得主解讀 CRISPR 的十年
- 《Nature》甲流當季,大腦如何感知感染以及“布洛芬”沒效果的原因?
- 修改mRNA或可治療阿爾茨海默病
- Immunity:免疫系統的“馬拉松選手”
資訊文章
您的瀏覽歷史