細胞編程,再現人類細胞獨特特征的神經網絡
摘要:對影響人類大腦的疾病的研究通常基于動物模型,無法再現人類神經疾病的復雜性。因此,這些方法在臨床環境中應用于患者時往往失敗。在這種情況下,利用皮膚細胞產生人類神經元培養的細胞重編程技術的發現,徹底改變了神經科學創新療法的研究和發展。
發表在《Stem Cell Reports》雜志上的一項研究表明,這種細胞重編程方法允許創建神經網絡,這種神經網絡可以復制人類細胞的獨特特征——不同于從嚙齒動物細胞中獲得的特征——具有提醒人類大腦發育的臨時動態。因此,基于重新編程的人類細胞的細胞模型可以促進對抗神經疾病的新有效療法的發展,同時減少在實驗室中實驗動物的使用。

圖1 細胞重編程方法允許創建神經網絡,可以復制人類細胞的獨特特征(圖源:[1])
這項研究由來自醫學與健康科學學院、巴塞羅那大學神經科學研究所和IDIBAPS的研究員Daniel Tornero Prieto領導。來自物理系和UB復雜系統研究所(UBICS)的研究人員Jordi Soriano Fradera和Estefanía Estévez-Priego以及來自隆德大學(瑞典)的Zaal Kokaia等人也參與了這項研究。
細胞重編程以克服動物模型的局限性
布法羅大學生物醫學系的Daniel Tornero指出,盡管我們與大多數哺乳動物共享大部分基因組,但“我們的細胞與其他物種(如嚙齒動物)的細胞之間存在相當大的差異,這些物種被用作大多數病理的動物模型,特別是,大腦中存在非常顯著的差異,特別是在組織和連通性方面。這使得我們的認知能力如此不同,這也解釋了為什么導致影響我們大腦的病理的缺陷在這些動物的大腦中不能以相同的方式復制。”
2007年,山中伸彌(Shinya Yamanaka)開發了基于誘導人類多能干細胞(hiPSCs)的細胞重編程技術,可以克服動物模型研究的局限性。這是一種可以從成年人的細胞中產生任何類型細胞的培養方法,相對簡單、有效且沒有相關的倫理考慮,在細胞治療和再生醫學的臨床應用中具有巨大潛力。
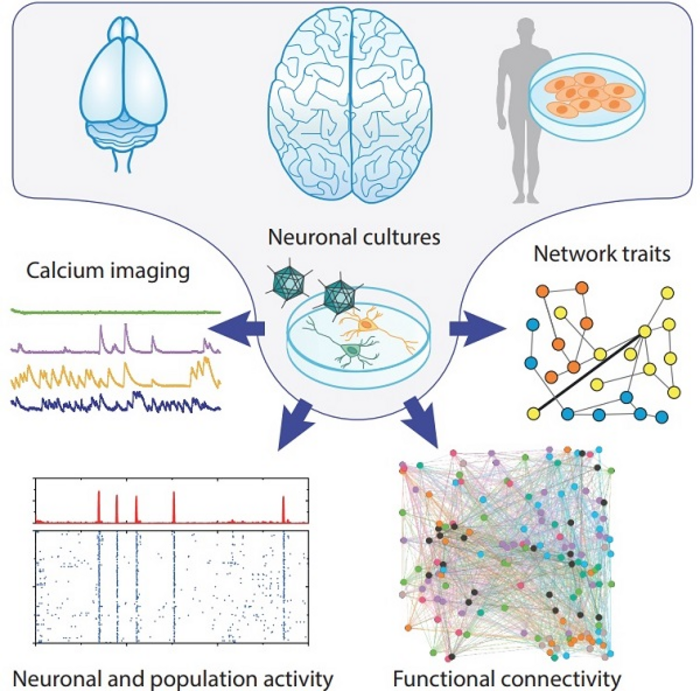
圖2 研究小組應用了細胞內鈣水平記錄技術,比較了用細胞重編程技術從人類細胞中獲得的神經元培養物與從嚙齒動物和人腦中獲得的神經元培養物的特性。(圖源:[1])
作為研究的一部分,研究小組應用了細胞內鈣水平記錄技術,比較了用細胞重編程技術從人類細胞中生成的神經元培養物與從嚙齒動物和人類大腦中獲得的神經元培養物的特性。這項技術提供了一種間接測量神經元活動的方法:在神經沖動從一個神經元傳遞到下一個神經元期間,鈣水平以一種特有的方式上升,可以通過細胞內鈣傳感器記錄下來。
該研究系統允許在整個培養過程中動態地對神經元活動進行高分辨率監測。實驗策略是通過使用特殊的板來完成的,這種板允許通過標記融入培養表面來跟蹤同一組細胞,這種技術可以最大限度地減少變量,并為神經網絡的研究產生更可靠和更有價值的結果。
不同神經回路之間的差異
這是該團隊第一次能夠研究和區分產生的不同神經元回路的特征,乍一看可能是相同的生物結構。結果表明,從功能的角度來看,人類起源的神經元在產生神經回路時表現不同。這些特征可能在一定程度上解釋了用于研究人腦病理的動物模型所存在的問題。
“首先,最讓我們震驚的是決定神經網絡生成和成熟的時間尺度。來自人類細胞的培養顯示出豐富而漸進的動態行為,因此從培養的20天到45天,可以清楚地觀察到生成的神經元網絡的成熟過程,”Daniel Tornero說。研究人員補充說:“在此期間,多虧了我們開發的不同描述符,我們已經能夠分析神經網絡如何隨著時間的推移而變得越來越復雜,因為人類神經元彼此之間的連接越來越多。”
此外,人類神經元能夠在培養物中建立更長時間的連接,這是由它們的生物學特性決定的,因為人類的大腦比嚙齒動物的大腦大得多。
Tornero說:“然而,由嚙齒動物細胞產生的神經回路在很短的時間內表現出單調的行為,在整個進化過程中幾乎沒有變化。”
安全協議和兼容的細胞庫
基于重編程人類細胞的細胞模型正在成為動物研究和臨床應用之間的相關中間步驟。基于重新編程的人類細胞生成這些用于疾病研究的細胞模型已經在臨床前研究中得到了很好的建立——2D培養或芯片上的器官系統(OoCs) 。最近,在基于使用生物材料、類器官或生物打印的3D系統中得到了很好的建立。
在再生醫學中,該技術在細胞治療策略中的應用顯示出巨大的潛力,并且在各種病理(1型糖尿病、心肌梗死、脊髓損傷、黃斑變性、帕金森病等)上進行了許多臨床試驗。建立安全可靠的方案和生成與人群中存在的不同異體群體兼容的細胞庫是這一研究領域最雄心勃勃的挑戰之一。
Daniel Tornero說:“這些新方法對于臨床前驗證不同的治療方法非常有價值,特別是在研究影響基于神經元回路組織的復雜過程的病理時(神經發育疾病、自閉癥譜系障礙、神經退行性病理等)。此外,基于人類多能干細胞誘導的細胞重編程將有可能生成患者特異性模型,并使用基因編輯工具(如CRISPR/Cas9技術),有可能獲得導致病理的突變被糾正的控制細胞,”研究人員總結道。
參考資料:
[1] Long-term Calcium Imaging Reveals Functional Development in hiPSCderived Cultures Comparable to Human but not Rat Primary Cultures
 |
 |
 |
| 官網:www.baichuan365.com | 微信服務號:iseebio | 微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn | 微信訂閱號:seebiotech | 泉養堂:www.canmedo.com |
此文關鍵字:細胞編程
相關資訊
- 切條機 CM3020
- 又一COVID-19潛在藥物有望上市,GSK/Vir提交單抗VIR-7831緊急使用授權申請
- 禮來GLP-1受體激動劑Trulicity大規模長期心血管預后研究顯著降低MACE事件風險
- 木薯淀粉
- 德國德樂 NBB-增菌培養液(NBB-B-AM)
- 研究發現兩種淀粉樣β蛋白抗體可引起小鼠神經功能障礙
- 有效率97%,AAV5基因療法可不受免疫系統影響
- Nat Biotechnol:新研究拓寬堿基編輯器的靶向范圍
- DAAs市場引多家藥企“廝殺” 中國迎來丙肝治愈新時代?
- 重組PI 3-激酶
新進產品
同類文章排行
- 細胞編程,再現人類細胞獨特特征的神經網絡
- Science子刊最新研究找到了新冠病毒令人失去嗅覺的關鍵原因
- 研究人員發現了導致COVID-19的病毒進入細胞的新途徑
- 清除人體內衣原體感染的關鍵鑰匙
- iScience:一種對抗遺傳性神經系統疾病的潛在途徑
- 真的有可以中和所有已知COVID-19毒株的抗體?
- 細胞“廢物”使抗癌的免疫細胞恢復活力!
- 男性注意!這種食品攝入過多會導致結直腸癌
- 無路可退!主食中的農藥殘留,可誘發阿爾茨海默病
- Cell出乎意料新發現:原來是這種“瀕死體驗”讓癌細胞惡化
資訊文章
您的瀏覽歷史