近日,來(lái)自芬蘭、瑞士、英國(guó)的一個(gè)研究小組在《自然-通訊》上發(fā)表文章,首次通過(guò)激活細(xì)胞自身的基因,成功將皮膚細(xì)胞轉(zhuǎn)化為多能干細(xì)胞。據(jù)報(bào)道,該研究小組使用了一類CRISPRa基因編輯技術(shù),該技術(shù)不切割DNA,可以在不改變基因組的情況下激活基因表達(dá)。到目前為止,只有通過(guò)向皮膚細(xì)胞內(nèi)人工引入一組名為Yamanaka因子的關(guān)鍵基因,才有可能激活細(xì)胞重編程,實(shí)現(xiàn)皮膚細(xì)胞向干細(xì)胞轉(zhuǎn)化。
這篇文章的題目為:Human Pluripotent Reprogramming with CRISPR Activators(用CRISPR激活劑進(jìn)行人類多能性重編程)。
在文章中,研究人員寫(xiě)道:基于CRISPR-Cas9的基因激活(CRISPRa)是一種很有吸引力的細(xì)胞重編程應(yīng)用工具,因?yàn)樗哂懈邚?fù)用容量和直接靶向內(nèi)源性基因座的能力。在該項(xiàng)研究中,我們利用CRISPRa靶向內(nèi)源性的OCT4、SOX2、KLF4、MYC和LIN28A的啟動(dòng)子,將原代皮膚細(xì)胞誘導(dǎo)成了多能干細(xì)胞(ipsCs)。通過(guò)額外地靶向涉及胚胎基因組激活的基因附近的一個(gè)保守Alu基序(EEA-motif),重編程效率可以提高一個(gè)數(shù)量級(jí)。這種效應(yīng)在某種程度上是通過(guò)NANOG和REX1的更有效激活來(lái)介導(dǎo)的。
這些數(shù)據(jù)表明,人類體細(xì)胞可以僅使用CRISPRa技術(shù)被重新編程為ipsCs。此外,這些結(jié)果揭示了EEA(EGA富集的Alu基序)基序相關(guān)機(jī)制在細(xì)胞重編程中的作用。
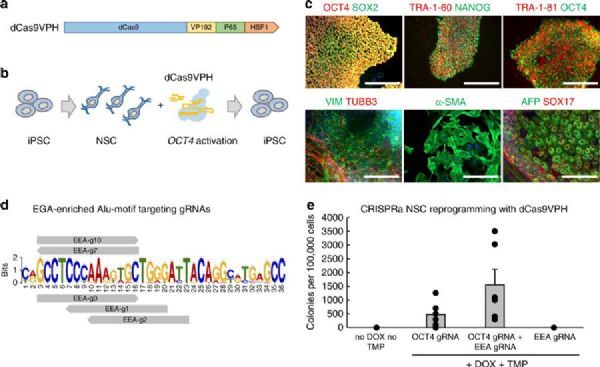 圖.CRISPRa介導(dǎo)的NSCs重編程和EEA基序靶向 a、dCas9VPH結(jié)構(gòu)示意圖.b、采用dCas9VPH介導(dǎo)的OCT4激活將NSC重編程為iPSCs。c、多能性標(biāo)志物的檢測(cè)及胚狀體的三系分化。d、用SpdCas9 gRNAs靶向EGA富集Alu基序。e、定量檢測(cè)由NSCs誘導(dǎo)的iPSC樣堿性磷酸酶陽(yáng)性克隆。
圖.CRISPRa介導(dǎo)的NSCs重編程和EEA基序靶向 a、dCas9VPH結(jié)構(gòu)示意圖.b、采用dCas9VPH介導(dǎo)的OCT4激活將NSC重編程為iPSCs。c、多能性標(biāo)志物的檢測(cè)及胚狀體的三系分化。d、用SpdCas9 gRNAs靶向EGA富集Alu基序。e、定量檢測(cè)由NSCs誘導(dǎo)的iPSC樣堿性磷酸酶陽(yáng)性克隆。
赫爾辛基大學(xué)Timo Otonkoski博士表示,CRISPR/Cas9可用于激活基因,這為細(xì)胞重編程帶來(lái)了一個(gè)很有吸引力的可能性,因?yàn)榭梢栽谕粫r(shí)間靶向多個(gè)目標(biāo)基因。基于內(nèi)源性基因激活而不是通過(guò)轉(zhuǎn)基因過(guò)表達(dá)的重編程在理論上也是控制細(xì)胞命運(yùn)的更具生理性的方式,并可能獲得更多的正常細(xì)胞。在這項(xiàng)研究中,我們展示了有可能設(shè)計(jì)一個(gè)CRISPR激活系統(tǒng),進(jìn)行強(qiáng)大的ipsCs重編程。
研究人員表示,實(shí)現(xiàn)成功的一把重要鑰匙是激活一個(gè)關(guān)鍵的遺傳元件,該元件被發(fā)現(xiàn)在受精后調(diào)節(jié)人類胚胎發(fā)育的最早期步驟。利用這一技術(shù),研究人員獲得了與非常典型的早期胚胎細(xì)胞非常相似的多能干細(xì)胞。
該研究還發(fā)現(xiàn),通過(guò)選址意向靶細(xì)胞類型的典型遺傳元件,可能能夠改善許多其他重編程任務(wù)。該研究的第一作者Jere Weltner博士表示,這項(xiàng)技術(shù)可能在生物樣本庫(kù)及許多其他組織技術(shù)應(yīng)用方面得到實(shí)際應(yīng)用。此外,該研究也揭示了控制早期胚胎基因激活相關(guān)機(jī)制的新見(jiàn)解。
原文出處:
New CRISPR Approach Converts Skin Cells into Pluripotent Stem Cells
 |
 |
 |
| 官網(wǎng):www.baichuan365.com |
微信服務(wù)號(hào):iseebio |
微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn |
微信訂閱號(hào):seebiotech |
泉養(yǎng)堂:www.canmedo.com |